یک مطالعه آزمایشگاهی جدید، به شکلی منحصربهفرد از متابولیسم گلیوبلاستوما بهره گرفت تا اثربخشی شیمیدرمانی و پرتودرمانی برای درمان سرطان مغز را افزایش دهد و ویژگیهای خودِ سرطان را علیه آن به کار گیرد.
به گزارش دیجینوی، پژوهشگران این مطالعه در راستای درمان سرطان مغز معتقدند که تغییر رژیم غذایی از یک نقطه ضعف متابولیکی کلیدی در سرطان بهرهبرداری میکند. در ضمن یافتههای آنها نشان میدهد که این رویکرد در صورت ترکیب با شیمیدرمانی و پرتودرمانی، موجب افزایش طول عمر در موشها میشود.
این مطالعه که در تاریخ ۳ سپتامبر (۱۲ شهریور) در نشریه «نیچر» (Nature) منتشر شده، نشان میدهد که درک عمیقتر از نحوه تنظیم متابولیسم سلولهای توموری در مسیر رشد بیوقفه میتواند فرصتهای درمانی جدیدی را برای این سرطان بهشدت مرگبار فراهم کند.
سلولهای سالم مغز برای حفظ فهرست گستردهای از عملکردهای خود (مانند انتقال الکتریکی و آزادسازی پیامرسانهای شیمیایی) به سوخت نیاز دارند؛ اما سلولهای سرطانی این فرآیندهای طبیعی را کنار میگذارند و خود را بهگونهای بازبرنامهریزی میکنند که به «سلولهای حرفهای تقسیمشونده» تبدیل شوند. این تغییرات برای پژوهشگران سرطان بسیار مهم هستند، زیرا ممکن است به درمانها اجازه دهند بین سلولهای سالم و سلولهای توموری تمایز قائل شده و در نتیجه درمانها هدفمندتر شوند.
کاستاس لیسیوتیس، (Costas Lyssiotis) استاد انکولوژی در دانشگاه میشیگان و یکی از نویسندگان این مطالعه، در گفتوگو با «لایو ساینس» (Live Science) گفت:
هنر واقعی در ارائه درمان سرطان این است که طوری عمل کنید سرطان بسیار بیشتر از سلولهای طبیعی از بین برود.
پژوهش مذکور به بررسی این موضوع پرداخته که چگونه گلیوبلاستوما متابولیسم را در مغز انسان و حیوان تغییر میدهد. این مطالعه با رویکردی بلندپروازانه، تحقیقات آزمایشگاهی را با عمل بالینی ترکیب کرد و بخشی از دادههای خود را از بافتهای مغزی بیماران تحت جراحی سرطان بهدست آورد. اجرای این تحقیق نیازمند همکاری میان متخصصان جراحی مغز انسان و جوندگان، مسیرهای متابولیکی و تحلیلهای مولکولی بود.
پروتکل از چند ساعت پیش از جراحی آغاز شد. به بیماران محلولی از گلوکز تزریق شد که با برچسبگذاری خاصی همراه بود تا از طریق تکنیکهای تحلیل مولکولی، قابل شناسایی باشد. این گلوکز در جریان خون آنها با حرکت گردشی در جریان بود و وارد سلولهای سالم و سرطانی مغز شد.
یکی از روشهای رایج در جراحی گلیوبلاستوما این است که علاوه بر برداشتن تومور، بخشی از بافت اطراف مغز نیز خارج شود تا خطر رشد مجدد سرطان کاهش یابد. تیم تحقیقاتی در طول جراحی هر ۳۰ دقیقه یک بار نمونه خون گرفتند و سپس بافتهای توموری و سالم برداشتهشده را منجمد کردند تا برای تحلیلهای بعدی آماده شوند.
سلولهای استخراجشده، گلوکز را متابولیزه کرده بودند و پژوهشگران مسیر حرکت این مولکولها را درون سلولها دنبال کردند. آنها توانستند با انجام آزمایشهایی بر روی موشها، دید واضحی از تفاوت عملکرد سلولهای توموری در هنگام مصرف قند بهدست آورند.
سلولهای سالم، گلوکز را برای فرآیندهایی مانند تنفس سلولی متابولیزه میکنند؛ فرآیندی که در آن قند و اکسیژن به سوخت مورد نیاز سلول تبدیل میشوند. در ضمن این سلولها گلوکز را به آمینواسیدی به نام «سرین» تبدیل میکنند که یکی از اجزای کلیدی در ساخت مولکولهای مهم پیامرسان عصبی بهشمار میرود.
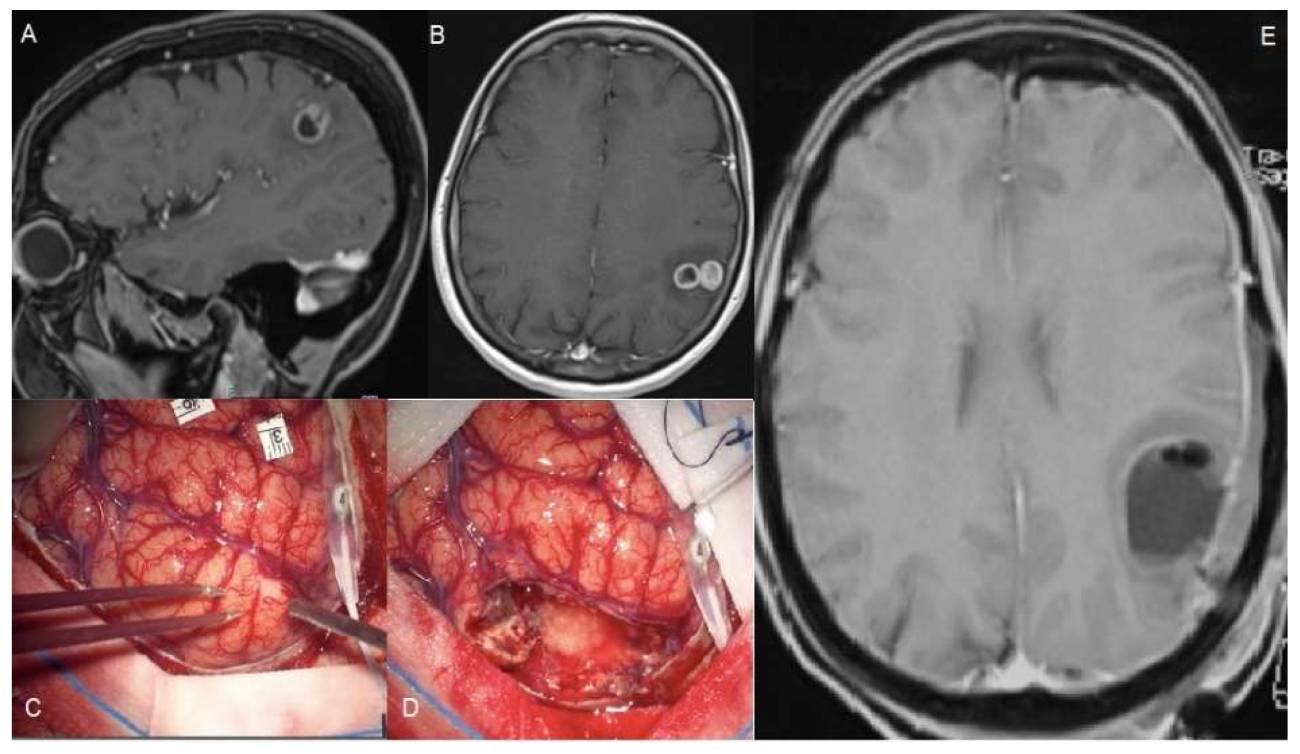 جراحی گلیوبلاستوما
جراحی گلیوبلاستوما
درمانهای شیمیپرتویی با هدف تخریب DNA سلولهای سرطانی عمل میکنند، اما مسیر متابولیکی جدیدی که سلولهای توموری در پیش میگیرند، منبع پایداری از نوکلئوتیدها برای ترمیم آسیبها را در اختیارشان قرار میدهد. نتایج مطالعه نشان داد که سلولهای توموری به منظور تقویت بیشتر رشد خود، سرین را نیز از بافتهای اطراف جذب میکنند.
دکتر وال و تیمش در این برهه زمانی، فرصت جدیدی را شناسایی کردند. آنها موشهایی را که سلولهای سرطانی انسانی به آنها پیوند زده شده بود، تحت رژیم غذایی خاصی قرار دادند که میزان سرین دریافتی را بهشدت کاهش میداد. به اعتقاد لیسیوتیس، ممکن است این رویکرد با استفاده از رژیم کمپروتئین همراه با شیکهای پروتئینی فاقد سرین، در بیماران انسانی نیز قابل اجرا باشد.
پژوهشگران مجبور شدند با کاهش دسترسی سلولهای توموری به سرین، متابولیسم گلوکز را دوباره به سمت تولید سرین هدایت کنند. این تغییر باعث کاهش تولید نوکلئوتیدها شد و سلولهای سرطانی را نسبت به شیمیپرتودرمانی آسیبپذیرتر کرد. موشهایی که این ترکیب درمانی را دریافت کردند، نسبت به موشهایی که فقط تحت شیمیپرتودرمانی قرار گرفته بودند، بیشتر زنده ماندند.
لیسیوتیس توضیح داد که این نقطهضعف احتمالاً تنها برای مدت محدودی مؤثر خواهد بود؛ زیرا سلولهای گلیوبلاستوما توانایی بالایی در سازگاری با تغییرات متابولیکی دارند. علاوه بر این، برخی از سلولهای توموری کمتر از سایر سلولها به سرین جذبشدند.
او در رابطه با این موضوع چنین گفت:
اگر بتوانید آن نقطه طلایی را پیدا کنید (یعنی آنها را از سرین محروم و همزمان درمان را آغاز کنید) میتوانید قبل از اینکه راهحلی برای مقابله پیدا کنند، آنها را هدف قرار دهید.
در همین راستا، دکتر وال کار روی یک مطالعه بالینی پیگیری را آغاز کرده است تا نتایج بهدستآمده از آزمایشهای موشها را با دادههای بیماران انسانی مبتلا به سرطان تأیید کند:
امیدواریم بتوانیم این روش را تا پایان امسال یا اوایل سال آینده در اختیار بیماران قرار دهیم. این کار با چالشهایی همراه خواهد بود و نیاز به هماهنگی دارد. طی کردن روند درمان سرطان بسیار دشوار است. ما از بیماران میخواهیم هر روز برای پرتودرمانی مراجعه کنند و شیمیدرمانی شوند. فکر میکنم تقاضا از آنها برای پیروی از یک رژیم غذایی خاص نیز میتواند چالشبرانگیز باشد.







